Dieser Beitrag ist auch verfügbar auf:
PMCF – Post-Market-Clinical-Followup
Das PMCF oder auch klinische Nachbeobachtung nach dem erstmaligen Inverkehringen eines Medizinproduktes, beschreibt den Prozess eines Unternehmens, der misst wie und ob ein Medizinprodukt im Rahmen seiner Zweckbestimmung, die nötige Leistungsfähigkeit aufweist. – Kurz gesagt, der Hersteller muss valide nachweisen, dass das Medizinprodukt wirkt!
Die Hersteller führen eine klinische Bewertung nach Maßgabe der in Artikel 61 und in Anhang XIV festgelegten Anforderungen durch, die auch eine klinische Nachbeobachtung nach dem Inverkehrbringen umfasst.
(Verordnung (EU) über Medizinprodukte 2017/745, Art. 10, Abs. 3)
Damit wird klar, dass Medizinprodukte immer einer nachgewiesen Wirkung nachgehen!
Sie sind Anwender der Luxxamed-Mikrostromtherapie und interssieren sich für eine Teilnahme an der Studie?
Dann schreiben Sie einfach ein kurze E-Mail an pw (at) luxxame.de – Studienteilnehmer werden mit der regelmäßigen Lieferung von Klebeeletroden in Form einer Aufwandsentschädigung unterstützt!
PMCF bei Luxxamed Mikrostromgeräten
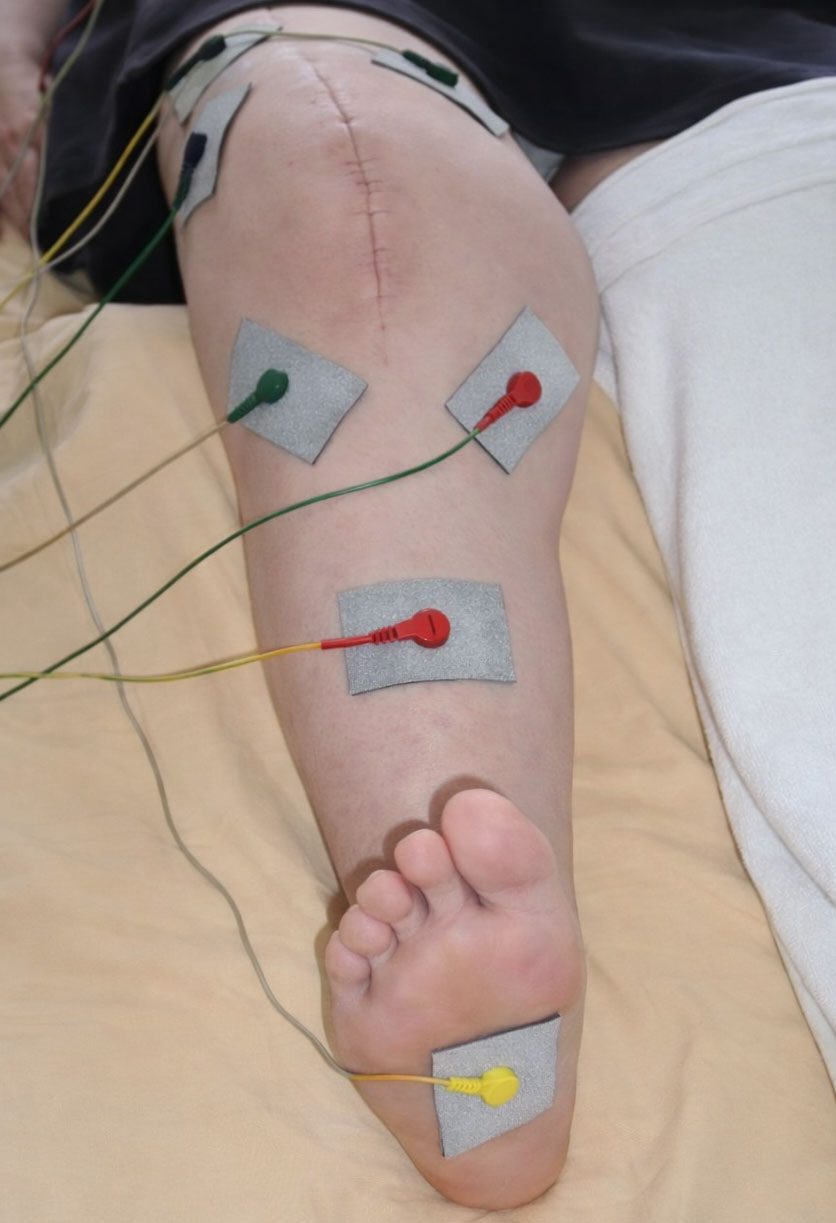
In der Luxxamed GmbH, als ISO 13485 zertifiziertes Unternehmen, setzen wir auf Studien, genauer gesagt Anwenderstudien. Hierzu können Anwender der Luxxamed Mikrostromgeräte (Ärzte, Physiotherapeuten, Heilpraktiker und Ergotherapeuten) an einer PMCF-Studie teilnehmen. Im internen Bereich der Internetseite der Luxxamed GmbH, haben wir hier eigens einen Fragebogen entwickelt.
Die Anwender benötigen für das digitale Ausfüllen des Fragebogens nicht mehr als 3-5 Minuten. Im Jahr 2021 wurde die letzte Auswertung aus insgesamt 1417 Einzelbehandlungen durchgeführt. ➡ Hier gehts zur Studie
« Back to Glossary IndexGemäß der MDR müssen die Hersteller eine klinische Bewertung sowie Nachbeobachtung nach dem Inverkehrbringung des Produktes durchführen (Verordnung (EU) 2017/745, Art. 10, Abs. 3). Eine klinische Bewertung ist für alle Medizinprodukte der Risikoklasse IIa und ohne Ausnahme notwendig. Sie muss nach einem zuvor durch den Hersteller genau definierten Verfahren durchgeführt werden. Die Grundsätze dieses Verfahrens zur Bewertung der klinischen Leistungsfähigkeit sind eine kritische Bewertung von wissenschaftlicher Fachliteratur und ein Nachweis darüber, dass das zu bewertende Produkt mit dem Produkt, auf das sich die Daten der wissenschaftlichen Fachliteratur beziehen, äquivalent ist. Grundlage für die Feststellung der Äquivalenz sind die Zweckbestimmung der Produkte sowie die Sicherheits- und Leistungsanforderungen, die gleichartig sein müssen. Daneben werden in Anhang XIV der MDR weitere Merkmale genannt, die zur Bewertung der Gleichartigkeit von Medizinprodukten im Rahmen einer klinischen Bewertung herangezogen werden müssen. Dort heißt es, dass die Produkte technisch und biologisch gleichartig sein müssen. Technische Äquivalenz bedeutet, dass die Bauart, die Spezifikationen und die physikalisch-chemischen Eigenschaften der Produkte, z. B. deren Energieabgabe oder die zugrunde liegenden Software-Algorithmen, gleichartig sein müssen. Auf biologischer Ebene ist die Vergleichbarkeit im Kontakt und im Umgang mit menschlichen Geweben und/oder Körperflüssigkeiten zu bewerten. Letztes Äquivalenzkriterium sind der klinische Einsatz und die klinische Wirkung. Diesbezüglich werden Patientenpopulationen und die Auslobung der Wirkungsweise verglichen (Verordnung (EU) 2017/745, Anh. XIV, Teil A, Abs. 3).
Im Guideline-Dokument, MEDDEV 2.7/1 revision 4, Anhang A1, das im Juni 2016 von der Europäischen Kommission veröffentlicht wurde, werden weitere Kriterien für die Bewertung der Äquivalenz von Produkten benannt.
Die Äquivalenz kann immer nur zu einem Produkt hergestellt werden, und alle drei Arten von Äquivalenz, klinische, technische und biologische, müssen gleichermaßen gegeben sein. „Gleichartig“ bedeutet im Sinne des MEDDEV 2.7/1 revision 4, dass es keine signifikanten Unterschiede in der Leistung und der Sicherheit der zu vergleichenden Geräte gibt. Ersichtliche und nichtersichtliche Unterschiede zwischen den Geräten müssen vollständig ausgearbeitet und offengelegt werden. In diesem Zusammenhang ist zu prüfen, inwieweit diese einen Einfluss auf die klinische Leistung und die klinische Sicherheit der Geräte haben können. Es muss ebenfalls vom Hersteller untersucht werden, inwiefern bei den beiden zu vergleichenden Produkten die verwendeten Materialien und ggf. deren Verarbeitung voneinander abweichen. Dies kann einen Einfluss auf die biologischen Eigenschaften haben und daher die Gleichartigkeit in der medizinischen Wirkung der Geräte beeinflussen. Ob dies der Fall ist, muss ermittelt, dokumentiert und bewertet werden. Bei Medizinprodukten, bei denen Messungen vorgenommen werden können, müssen diese aufgezeichnet und mit denjenigen der Äquivalenzprodukte verglichen werden. Technische Zeichnungen und bildliche Darstellungen sind ebenfalls in die Bewertung mit aufzunehmen. In Bezug auf die technische Auslegung der Geräte untereinander muss die Gleichartigkeit auch auf hinsichtlich der technischen Merkmale gegeben sein. Geräte, die die gleiche medizinische bzw. therapeutische Wirkung haben, sind bei unterschiedlichen technischen Vorgehensweisen nicht miteinander vergleichbar. Grundsätzlich ist nach MEDDEV 2.7/1 die Äquivalenz von Medizinprodukten nur dann gegeben, wenn bei einem CE-gekennzeichneten Produkt die gewonnenen klinischen Daten entsprechend der in der Gebrauchsanweisung genannten Zweckbestimmung angefallen sind (MEDDEV 2.7/1 rev. 4, 2016, S. 33).
Sollte über den Weg der klinischen Bewertung die Konformität des Medizinproduktes, bezogen auf die klinische Leistungsfähigkeit, durch den Hersteller nicht nachweisbar sein, besteht die Möglichkeit, sie über den Weg einer klinischen Prüfung zu belegen. Johner (2018) schreibt mit Bezug auf klinische Prüfungen von Medizinprodukten: „Klinische Prüfungen von Medizinprodukten versuchen die meisten Hersteller um jeden Preis zu vermeiden. Kein Wunder: Eine klinische Prüfung ist zeit- und kostenintensiv, und die regulatorischen Anforderungen daran umfangreich und komplex.“ (Johner, 2018a)
Der Prozess der klinischen Bewertung muss über den gesamten Produktlebenszyklus hinweg erfolgen und über die Festlegung eines Prozesses für die klinische Nachbeobachtung durch den Hersteller kontinuierlich aktualisiert werden (Verordnung (EU) 2017/745, Kap. VI, Art. 61.). Eine klinische Bewertung muss demnach auch dann durchgeführt werden, wenn der Hersteller eine klinische Prüfung durchführen muss.
(Walitschek, 2018)